Cuando se trata de gas natural, no debe estar familiarizado con él, y hoy en día ningún hogar puede cocinar sin él. El componente principal del gas natural es el metano, que es uno de los compuestos de hidrocarburos más simples. Acelerar el desarrollo y la utilización del metano es la clave para realizar el desarrollo verde y sostenible de la industria energética y química. Además de su uso directo como combustible, el metano también se puede usar como recurso C1, es decir, una molécula que contiene un átomo de carbono y puede continuar convirtiéndose para preparar productos químicos de alto valor agregado, como metanol, fórmico, fórmico. ácido y así sucesivamente. El metano se puede quemar en oxígeno para formar agua y dióxido de carbono. Sin combustión, ¿es posible activar y convertir los enlaces de hidrocarburos de las moléculas de metano en condiciones suaves? ¡La respuesta es sí! Esta es la reacción del "santo grial" en el campo de la catálisis. Las reacciones asociadas con el "santo grial" a menudo son extremadamente desafiantes, ya que es posible que necesiten llevarse a cabo en condiciones muy duras, o pueden necesitar superar las dificultades inherentes de una reacción química, como la activación de compuestos altamente estables, bajos rendimientos y baja selectividad. Estos desafíos dificultan la realización de estas reacciones, pero si se pueden lograr con éxito, conducirán a avances significativos en la investigación científica y las aplicaciones industriales.

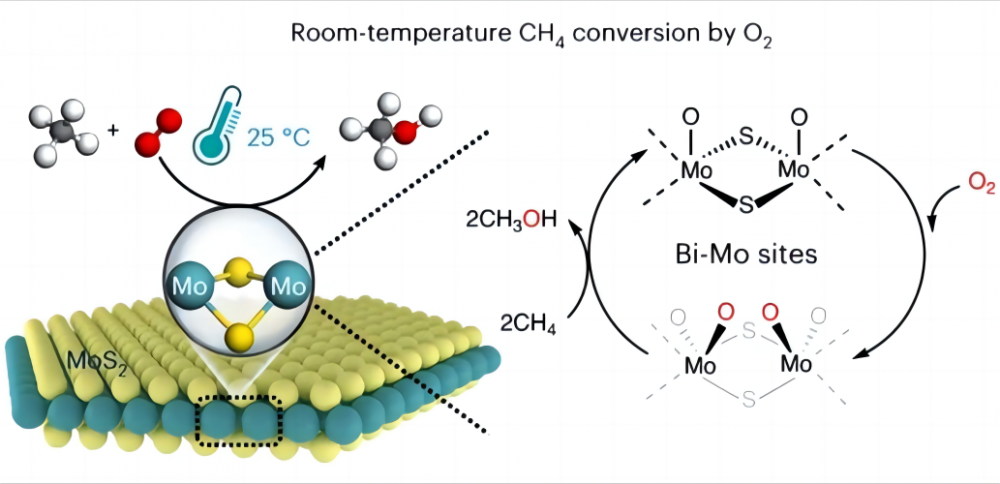
1. Calles en la conversión de metano a bajas temperaturas Es muy difícil convertir metano directamente a otros productos químicos útiles con oxígeno económico a bajas temperaturas o incluso temperatura ambiente, ¿por qué es eso? Veamos la naturaleza del metano y el oxígeno. La estructura química del metano contiene cuatro enlaces idénticos de hidrógeno de carbono (CH) que forman una configuración ortotraídral altamente simétrica, y cada enlace CH3-H de metano tiene una energía de enlace de hasta 435 kJ/mol. Podemos pensar en el enlace CH de metano como una primavera particularmente fuerte. Esta primavera es muy tensa y requiere mucha fuerza para estirarse. En química, esta "fuerza" es la energía requerida para romper el enlace CH. Esta alta energía de unión hace que los enlaces CH de metano se estén termodinámicamente estable y muy difícil de descomponer o reaccionar con condiciones normales. Por otro lado, en las reacciones químicas, los grupos reactivos generalmente se generan bajo interacción polar (la interacción polar es el fenómeno de que una molécula tiene un extremo cargado positivamente y el otro cargado negativamente), mientras que la estructura simétrica y la naturaleza no polar de la molécula de metano previenen Al generar dicha polaridad (según la configuración molecular, una molécula con un plano de simetría no tiene polaridad) y no puede proporcionar grupos reactivos. Por lo tanto, la activación y conversión de metano es muy desafiante y generalmente requiere condiciones duras, como altas temperaturas (600-1100 ° C) o algunos "extremófilos", como ácidos súper fuertes y radicales libres para ayudar en la activación del metano. Por lo tanto, la principal dificultad para realizar la activación a baja temperatura del metano y el oxígeno radica en cómo activar el enlace CH de metano, es decir, cómo estirar el "resorte" en el enlace CH. 2. El milagro del catalizador A los científicos se les ocurrió una buena solución a este problema, y eligieron usar un catalizador para ayudar a activar el metano a bajas temperaturas (un catalizador es un químico que no cambia antes o después de una reacción, pero acelera la reacción alterando la cantidad mínima. de energía que debe inyectarse para que tenga lugar la reacción). En 2023, la catálisis de la naturaleza de la revista informó sobre el proceso de lograr la conversión directa de metano con oxígeno a los óxidos C1 (metanol (CH3OH), ácido fórmico (HCOOH) y metilenglicol (HOCH2OH)) usando un disulfuro de molibdonum específico (MOS2) catalizador a 25 ° C. Se logró una conversión de metano de 4,2% y casi 100% de oxigenatos C1 convirtiendo el metano y el oxígeno en valiosos oxigenados C1 en condiciones ambientales. Este MOS2 es el único catalizador informado hasta ahora que puede darse cuenta de la conversión de temperatura ambiente de metano y oxígeno. Todo esto se debe a la geometría única y la estructura electrónica del sitio MO en el borde del MOS2. Este sitio de Mo tiene una alta actividad de activación hacia el oxígeno en un entorno acuoso, formando la especie mágica O = Mo = O*. Esta especie hace que el enlace de hidrógeno de carbono sea más fácil de romper y reduce la energía de activación del enlace CH de metano, aumentando en gran medida la reactividad del metano y, por lo tanto, se da cuenta de la activación a baja temperatura del metano y el oxígeno. Este descubrimiento traerá más posibilidades para la utilización de energía futura y la protección del medio ambiente, además de darnos una comprensión más profunda del increíble papel de los catalizadores y auxiliares.
3. Importancia estratégica significativa de la activación a baja temperatura del metano Al darse cuenta de la conversión catalítica directa de metano y oxígeno a temperatura ambiente, y convertir metano en el gas natural en otros productos químicos útiles, puede mejorar en gran medida la tasa de utilización del gas natural, reducir los desechos y proteger mejor el medio ambiente y darse cuenta del desarrollo sostenible de energía energética . En segundo lugar, como gas de efecto invernadero, el metano es solo superado por el dióxido de carbono en su contribución al calentamiento global. Si el metano se puede convertir en otras sustancias, puede ayudarnos a reducir la emisión de contaminantes del aire (por ejemplo, óxidos de carbono, óxidos de nitrógeno, óxidos de azufre, hidrocarburos y compuestos de éter) y aliviar la presión del calentamiento global.




